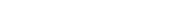【在某容积不变的密闭容器中放入一定量的NO2,发生反应2NO2(g)==N2O4(G)H<0.达到平衡后,若分别单独改变以下条件,下列判断正确的是A.升高温度,混合气体的颜色变浅B.通入NO2,化学平衡常数】
1人问答
更新时间:2024-04-27 15:15:06
问题描述:
在某容积不变的密闭容器中放入一定量的NO2,发生反应2NO2(g)==N2O4(G)H<0.
达到平衡后,若分别单独改变以下条件,下列判断正确的是
A.升高温度,混合气体的颜色变浅
B.通入NO2,化学平衡常数增大
C.通入NO2,重新达到平衡后混合气体的平均相对分子质量增大
D.增大压强,平衡向正反应方向移动,混合气体的颜色变浅
答案是C,已理解。关键是D选项,答案说“压强变大后,平衡向正反应方向移动,但C(NO2)增大,混合气体的颜色变深”。怎么也不清楚为什么压强变大后C(NO2)会变大,求解释!
其它推荐
其它推荐
最新更新
精品分类
优秀其它推荐
热门其它